Pancar kökü kırmızısı pancar köklerinden pres suyu olarak veya parçalanmış pancar köklerinin sıvı ekstraksiyonu sonucunda elde edilmektedir.
Özgün Yürük, Şükrü Karataş / İstanbul Aydın Üniversitesi Gıda Müh. Böl.
ozgunyuruk@stu.aydin.edu.tr /sukrukaratas@aydin.edu.tr
Özet
Bu araştırmada kırmızı pancarın ekstraksiyonundan elde edilen betanin renk maddesinin bir Brix’teki solüsyonlarının ışık altında ve farklı sıcaklıklarda bekletilmesi sonucu betaninin değişimi incelendi. Örnekler 500 ml’lık şişelerde 10-30˚C’lik sıcaklıklarda 3W’lık led ışık altında renk değişimleri. Tepkime hız sabitleri 10, 20, 25 ve 30°C sıcaklık değişimlerine göre sırasıyla 0,0232, 0,058, 0,349 ve 0,6648 gun-1olarak spektrofotometrik metotla belirlendi. Ayrıca kinetic değişimlerinin birinci dereceden reaksiyona uyduğu ve aktivasyon enerjisinin 29,098 kcal/mol olduğu ve tepkime hız değişimi 30˚C’de 10˚C’ye göre 28 kat daha hızlı olduğu görüldü.
Anahtar kelimeler: Pancar, betanin, tepkime hız sabiti
Giriş
Pancar kökü kırmızısı pancar köklerinden pres suyu olarak veya parçalanmış pancar köklerinin sıvı ekstraksiyonu sonucunda elde edilmektedir. Betalain sınıfından renklendirici olarak başlıca pigmenti betanindir. Kırmızıdan koyu kırmızıya kadar konsantre sıvı, toz veya katı halde bulunmaktadır. Betaninin stabilite gösterdiği pH 4,5 iken pH 7 ve üzerinde olduğunda hızla bozulmaktadır. Kuru ortamda depolanan pancar kökü kırmızısı stabilken, sıvı çözeltilerde katımadde etkisi azaldıkça rengin stabilitesi azalmaktadır (Altuğ, 2009). Pigment stabilitesi, ısı, oksijenve pH gibi faktörlerden etkilenmektedir (Cemeroğlu, 2011). Betalainler birçok meyve ve sebzelerde bulunmaktadır. Kırmızı pancar çoğunlukla Kuzey Amerika, Orta Amerika ve İngiltere’de yetiştirilmektedir (Rebecca, Boyce ve Chandran 2010).
Betalainler yapılarına göre temel betasiyanin (kırmızı-mor) ve betaksantinler (sarı) olarak ayrılmaktadır. Temel betasiyanin pancarda betanin, betaksantinler ise vulgaksantin I ve II olarak belirtilmiştir (Anonim, 2018a ve Anonim 2018b). Betanin, isobetanin, probetanin ve neobetanin ile birlikte bir betalain pigmenti olup ayrıca pancardaki diğer pigmentler, indoksantin ve vulgoksantindir (Anonim 2018a). Pancardaki başlıca betasiyanin, betanindir ve kırmızı pigmentin % 75-95’ini oluşturmaktadır (Chandran, Nisha, Singkal ve Pandit, 2014).

Betaninin ışığa bağlı bozulmanın, oksijene bağlı olduğu bildirilmiştir (Attoeve von Elbe, 1981). Işığın zararlı etkileri, anaerobic koşullar altında önemsiz bulunmuştur (Huangve von Elbe, 1986). Isı, gıda işleme ve saklama esnasında betalain kararlılığı üzerinde en önemli etki faktörü olarak görülmektedir. Betalainler yüksek sıcaklıklarda kararlılığını kaybeden ısıya dirençli pigmentlerdir. Von Elbe ve ark.,(1974), bu sırada bozunma hızı artan sıcaklık ve ısıtma etkisi ile hızlanmaktadır. (Saguy ve ark., 1978). Betalain kararlılığının, 50 ve 60°C, 70 ve 80°C (Havlíková ve ark., 1983), ya da 60 ve 75°C arasında belirgin bir düşüş gözlemlenmiştir (Saguy ve ark., 1978).
Betalainler gıdaları renklendirmek amacıyla kullanılan çevre koşullarına duyarlı pigmetlerdir. Betalainler pH ve sıcaklığa hassas olup sıvı ve toz halde bulunmaktadır. Dondurma, şekerleme, yoğurt ve tatlılara katılmaktadır. Betanin kurutulmuş halde pH aralığı 3,5-7.0 arası kararlı durumda bulunmaktadır (Anonim 2018b).

Yöntem ve metotlar
Kırmızı pancarın ekstraksiyonu
Kırmızı pancar market koşullarından alındıktan sonar dış tarafı soyularak küçük parçalar haline getirildi. 100g pancar numunesi için 250 ml safetil alkol ilave edildi. Numune blenderdan geçirilip ve 24 saat buzdolabında bekletildi. Filtre kâğıdından süzülen alkol pancar karışımının rotary evaporatörde etilalkolü uçuruldu. 50-55 brix arasında çıkan konsantre pancar numuneleri maltodekstrin eklenerek vakum altında 40°C’de kurutuldu (Attia veark., 2013).
Spektrofotometrede betanin incelenmesi
Kırmızı pancar konsantrelerine saf su eklenerek bir brixlik (Abbe Refraktometresi) numune elde edildi. Hazırlanan numuneler 500ml’lik kapaklı şişelere konuldu. 10°C derece için buzdolabı koşulunda 20, 25, 30°C dereceler için etüvde led ışık altına (3W) konularak bekletildi. Belirli zaman aralıklarında alınan numuneler küvete konuldu. 510 nm’lik dalga boyunda spektrofotometrede ölçüm yapıldı. Absorbans değerlerinin zamana bağlı değişimi belirlendi. Farklı konsantrasyonlarda hazırlanan pancar numuneleri 510 nm dalga boyu için ölçüm yapılarak kalibrasyon eğrisi oluşturuldu. Kırmızı rengin sıcaklıkla ve ışıkta renk stabilitesinin değişimi Lambert-Beer yasasına göre incelenerek k1 reaksiyon hız sabiti ve Aktivasyon(Eo) enerji değerleri hesaplandı (Labuza 1984).
Bulgular
Kırmızı rengin sıcaklıkla ve ışıkta renk stabilitesinin değişimi Lambert-Beer yasasına göre incelenerek k1reaksiyon hız sabiti ve Aktivasyon (Eo) enerji değerleri hesaplandı. Araştırmada iki paralel olarak çalışıldı ve ortalaması alındı.
Kalibrasyon grafiği ve regresyon denklemi excel ile oluşturuldu ve farklı konsantrasyonlara göre kalibrasyon eğrisi belirlendi (Şekil 1).
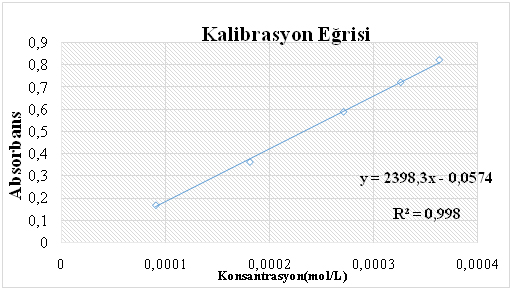
Şekil 1. Absorbans-Konsantrasyon Grafiği
Reaksiyon hızı, ilk olarak Arrhenius tarafından 1889’da parametrelendirilen artan sıcaklıkla birlikte artmaktadır. Spesifik olarak, sabit k oranı formüle göre artış göstermektedir (Burnham, 2017).
Arrhenius Denklemine (k=Ae-Ea/RT) göre Aktivasyon enerjisi hesaplanmıştır (Wright 2004).
A: Referans Faktörü
k: Tepkime Hız Sabiti
R: Gaz sabiti (1,987cal/molK veya 8,413J/molK)
T: Sıcaklık (Kelvin )
Ea: Aktivasyon Enerjisi(cal/mol veya J/mol)
Her sıcaklık için zamana bağlı k değerleri hesaplanarak Çizelge1-4’te gösterildiği gibidir. Zaman-ln(A) grafiği çizilerek eğimden k değerleri hesaplanmıştır. Daha sonar lnk değeri ile sıcaklık (1/T) arasında ilişkiden aktivasyon enerjisi hesaplanmıştır (Labuza 1984).
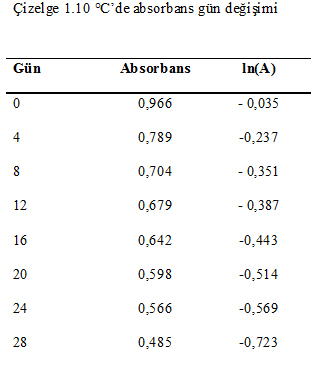
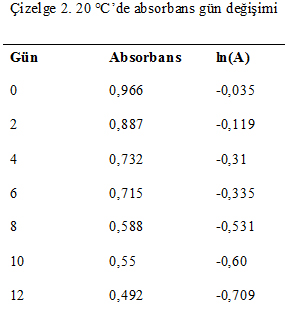

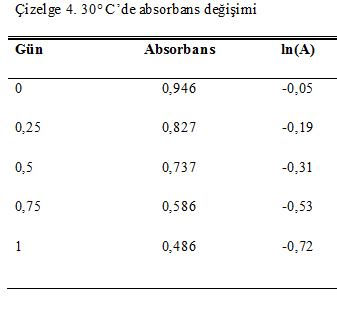


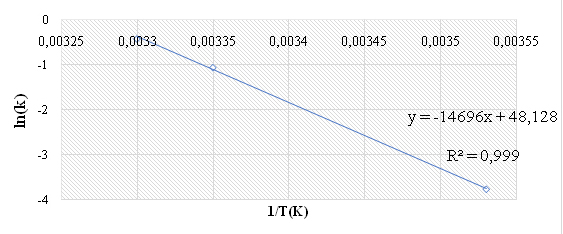
Şekil 2. Bir brixlik pancar suyu ln(k)-1/T(K) grafiği
Aktivasyon Enerjisi;
Eğim=-Ea/R
–14696= -Ea/1,98 Ea= 29098,08 cal/mol = 29,098 kcal/mol olarak hesaplandı.
Sonuç ve öneriler
Reaksiyonda k değerinin ln’leri alınarak grafiğin y eksenine bu değerlere karşılık olan sıcaklık değerleri ise Kelvin’e çevrilip resiprokali (1/T) de x eksenine yazılarak doğrusal eğri oluşturuldu. Regrasyon analizi oluşturulan eğriye uygulandı, grafiğin eğimi ile hız sabiti çarpılarak da aktivasyon enerjisi Arrhenius denklemiyle (Ea) hesaplandı, 1 brix için 29,098 kcal/mol olarak bulundu.
Saguy, Kopelman ve Mizrahi (1978) tarafından kırmızı pancarın 60, 75, 81 ve 86°C’de 4,86 mg/L konsantrasyonundaki betanin parçalanmasına ilişkin yapılan çalışmada aktivasyon enerjisi 20.4 kcal/mol olarak belirlenmiş bu çalışma bizim araştırmamızla paralellik göstermektedir.
Betanin’de sıcaklıkla betasiyanin bozunması kırmızı pancar ve mor pitaya sularında olduğu gibi birinci mertebeden reaksiyon kinetiğini takipettiği bildirilmiştir (Von Elbe ve ark., 1974; Saguy ve ark., 1978; Saguy, 1979). Kendi araştırmamızda kırmızı pancar suyu için reaksiyon kinetiği birinci dereceden bulundu. Araştırmamızla uyum içinde olduğu belirlendi.
Folyosuz cam kavanozlarda depolanan konsantrelerde betasiyanin ve betaksantin degradasyonuna ilişkin aktivasyon enerjisi değerleri sırasıyla 65 J/mol ve 89 J/mol ayrıca folyolu olan cam kavanozlarda depolanan konsantrelerinde ise 91 J/mol olarak bulunmuştur (Saguy ve ark., 1978). Aktivasyon enerjileri karşılaştırıldığında pancar suyundaki ısıyla renk değişim hızının depolama koşullarına göre daha yavaş oluştuğu, bunun da zamana bağlı olduğu düşünülmektedir.
25°, 35° ve 45°C sıcaklıklarda folyosuz cam kavanozlardaki pancar suyu konsantresinin depolanması sonrasında betasiyanin miktarının birinci derecere aksiyon kinetiğine göre kayba uğradığı belirlenmiştir (Kayın, 2014). Aynı örneklerdeki betaksantin miktarının da depolama sıcaklık ve süresine bağlı olarak birinci derecere aksiyon modeline göre kayba uğradığı gözlenmiştir.
Sonuç
Yapılan bu araştırmada kırmızı pancarın ekstraksiyonu sonucunda oluşan betanin renk maddesinin 1 Brix‘teki yapılan çalışmalarda, led ışık altında 10, 20, 25 ve 30°C sıcaklıklarda bekletilmesi sonucu betaninin değişimi; hız sabitleri sırasıyla 0,0232, 0,058, 0,349 ve 0,6648 gün-1 olarak belirlendi. En hızlı renk değişimi 25 ve 30°C’de olduğu belirlendi. Tepkime hız değişimi 1 Brix için 30˚C’de 10˚C’ye göre 28 kat daha hızlı olduğu belirlendi. Aktivasyon enerjisi (Ea) 29,098 kcal/mol olarak bulundu.
Betaninin renginin sıcaklık, ışığa karşı hassas olduğu belirlendi. Bu bağlamda marketlerde satılan kırmızı renkli ürünlerin özellikle soğuk zincirde satılan ürünlerin üzerine fazla miktarda ışıklandırma yapılmasının ürünün kırmızı rengine etki yaptığı belirlendi.
Kaynaklar
Altuğ T. (2009) Gıda Katkı Maddeleri Kitabı, üçüncü baskı
Azeredo, M.C. (2009)Betalains: Properties, Sources, Applications, and Stability – A Review International Journal of Food Science and Technology, 44, 2365-2376
Attia, Gamila ,Y., Moussa M.E.M. and Sheashea E.R, (2013). Characterization of Red Pigments Extracted from Red Beet (Beta Vulgaris, L.) and Its Potential Uses as Antioxidant and Natural Food Colorants Food Technology Research Institute. ARC, Giza, Egypt
Attoe, E.L,von Elbe, J.H., (1981) Photochemial degradation of betanine and selected anthocyanins. Journal of Food Science 50,106-110.
Burnham, A.K,(2017). Global Chemical Kinetics of Fossil Fuels, SpringerInternational Publishing AG p2
Chandran, J.; Nisha, P. Corresponding Author Rekha S. Singhal, and Pandit, A.B. (2014) Degradation of Colourin Beetroot (Beta Vulgaris L.): A Kinetics Study J Food Sci Technol. 2014 Oct; 51(10): 2678-2684.
Cemeroğlu, B.S.(2011)Meyve ve Sebze Teknolojisi Cilt 1, 2011 Ekim;117-119.
Huang, A.S, von Elbe, J.H., (1986) Stability comparison of two betacyanine pigments- amaranthine and betanine. Journal of Food Science 51, 670-674.
Kayın,N. (2014) Farklı Sıcaklıklarda Depolanan Kırmızı Pancar (Beta vulgaris) Suyu Konsantresinin Renk Stabilitesinin Belirlenmesi
Labuza, T.P. (1984)Application of chemical kinetics to deterioration of foods Journal of Chemical Education 61(4)
Rebecca, O.P.S; Boyce A.N. and Chandran S. (2010)Pigment Identification and Antioxidant Properties of Red Dragon Fruit (Hylocereus Polyrhizus). African Journal of Biotechnology Vol. 9(10), Pp. 1450-1454.
Saguy, Saguy, I;Kopelman,I.J. and Mizrahi S.(1978). Thermal Kinetic Degradation of Betanin and Betalamic J. Agric. Food Chem., Vol. 26, No. 2.
Saguy, I., (1979) Thermostability of red beet pigments (betanine and vulgaxanthin-I): Influence of pH and temperature. J. Food. Sci., 44: 1554-1555.
Von Elbe, J.H., I.Y. Maing and C.H. Amundson. (1974)Colour stability of betanin. J. Food Sci., 39: 334-337
Wright,R.,M. ,(2004). An Introduction to Chemical Kinetics
İnternet Kaynakları
Anonim, (2018a)http://www.foodcolor.com/beet-juice-color
Anonim, (2018b) http://www.food-info.net/uk/colour/beetroot.html






